Rumus Normalitas dalam Kimia Beserta Contohnya
Rumus Normalitas – Dalam dunia kimia, normalitas adalah salah satu ukuran konsentrasi larutan yang penting. Normalitas memberikan gambaran tentang jumlah ekivalen per satuan volume larutan. Untuk memahami konsep ini dengan lebih baik, penting untuk mengetahui rumus-rumus yang terlibat serta melihat contoh penggunaannya dalam kehidupan sehari-hari.
Apa Itu Normalitas?
Normalitas adalah salah satu ukuran konsentrasi larutan yang digunakan dalam kimia. Ini menggambarkan jumlah ekivalen zat terlarut per liter larutan. Normalitas sering digunakan dalam konteks reaksi kimia yang melibatkan pemindahan elektron atau reaksi asam-basa di mana perbandingan satu ekivalen zat terlarut dengan satu ekivalen zat reaktan sangat penting.
Konsep normalitas ini berbeda dengan molaritas, yang mengukur jumlah mol zat terlarut per liter larutan. Sedangkan normalitas menggambarkan jumlah ekivalen zat terlarut. Satu ekivalen adalah jumlah zat yang mengandung satu molekul terlarut atau satu mol dari zat terlarut yang direaksikan dalam suatu reaksi kimia tertentu. Oleh karena itu, normalitas memberikan gambaran yang lebih langsung tentang reaksi yang terjadi dalam larutan tersebut.
Penggunaan normalitas sering kali ditemui dalam analisis kimia, sintesis kimia, dan dalam menyiapkan larutan untuk digunakan dalam berbagai reaksi. Misalnya, dalam titrasi, di mana larutan standar dengan konsentrasi yang diketahui ditambahkan ke larutan sampel untuk menentukan konsentrasi suatu zat dalam sampel, normalitas digunakan untuk mengukur konsentrasi larutan standar dan larutan sampel.
Dengan demikian, normalitas merupakan konsep penting dalam kimia analitik yang memungkinkan para ilmuwan dan praktisi kimia untuk mengukur dan menyesuaikan konsentrasi larutan dengan tepat, terutama dalam konteks reaksi kimia yang melibatkan perubahan jumlah ekivalen zat terlarut.
Rumus Normalitas
Rumus untuk menghitung normalitas adalah sebagai berikut:
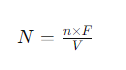
N adalah normalitas larutan (ekivalen/L).
n adalah jumlah ekivalen zat terlarut.
F adalah faktor normalitas atau jumlah ekivalen per satuan massa.
V adalah volume larutan (L).
Faktor normalitas (F) adalah jumlah ekivalen per satuan massa, dan nilainya dapat berubah tergantung pada jenis zat terlarut yang digunakan. Rumus ini penting dalam kimia analitik karena memberikan gambaran tentang konsentrasi larutan dalam konteks jumlah ekivalen zat terlarut per liter larutan. Dengan menggunakan rumus ini, kita dapat mengonversi konsentrasi larutan dari molaritas ke normalitas dan sebaliknya, yang penting dalam banyak aplikasi kimia, terutama dalam reaksi asam-basa dan reaksi redoks.
Contoh Penggunaan Rumus Normalitas
Sebagai contoh penggunaan rumus normalitas, pertimbangkan sebuah larutan HCl (asam klorida) dengan konsentrasi 0.5 Molar (M). Untuk menghitung normalitasnya, kita perlu mengetahui faktor normalitasnya. Dalam kasus HCl, faktor normalitasnya adalah 1, karena setiap molekul HCl memberikan satu ekivalen ion hidrogen (H⁺).
Jadi, jika kita memiliki larutan HCl 0.5 M, kita dapat mengonversi molaritasnya menjadi normalitas menggunakan rumus normalitas:
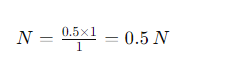
Ini berarti larutan HCl 0.5 M memiliki normalitas 0.5 N.
Sebagai contoh lain, pertimbangkan larutan NaOH (natrium hidroksida) dengan konsentrasi 1 M. Karena NaOH adalah basa kuat, faktor normalitasnya juga adalah 1. Jadi, larutan NaOH 1 M memiliki normalitas 1 N.
Dengan menggunakan rumus normalitas, kita dapat dengan mudah menghitung normalitas dari berbagai jenis larutan dan memahami konsentrasi larutan dalam konteks jumlah ekivalen zat terlarut per liter larutan. Hal ini sangat berguna dalam berbagai aplikasi kimia, terutama dalam reaksi asam-basa, titrasi, dan analisis kimia lainnya.
Kesimpulan
Normalitas adalah ukuran konsentrasi larutan dalam kimia yang menggambarkan jumlah ekivalen zat terlarut per liter larutan. Rumus normalitas adalah alat yang berguna dalam mengonversi konsentrasi larutan dari molaritas ke normalitas dan sebaliknya. Memahami konsep ini dan cara menghitungnya sangat penting dalam praktik kimia sehari-hari, terutama dalam reaksi asam-basa dan reaksi redoks.


